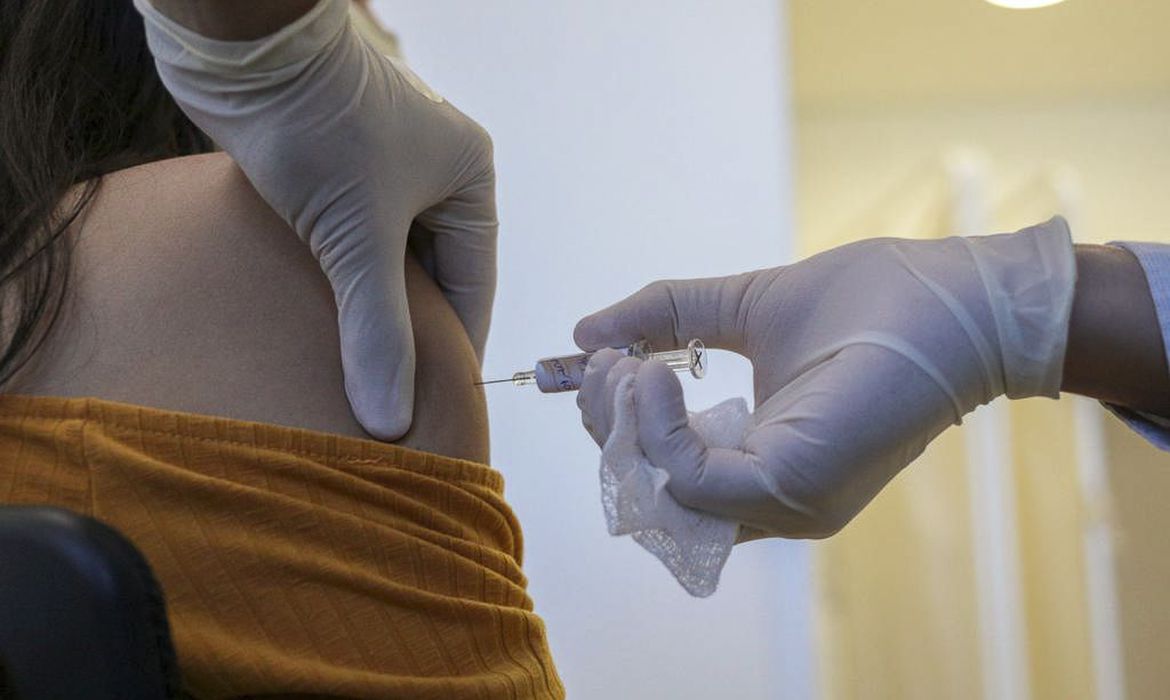
Após pressão, Anvisa libera importação de 6 milhões de doses da Coronavac
A agência, porém, ainda não se manifestou sobre o pedido de importação da matéria-prima para a fabricação de outras 40 milhões de doses. Pelo acordo entre...
Publicado em
Por Agência Estado

Após cobrança pública do Instituto Butantã, a Agência Nacional de Vigilância Sanitária (Anvisa) liberou nesta sexta-feira, 23, a importação de 6 milhões de doses da vacina Coronavac, desenvolvida pela farmacêutica chinesa Sinovac em parceria com a instituição brasileira.
A agência, porém, ainda não se manifestou sobre o pedido de importação da matéria-prima para a fabricação de outras 40 milhões de doses. Pelo acordo entre Sinovac e Butantã, 6 milhões de doses seriam entregues prontas ainda em outubro e o restante teria a produção finalizada no Brasil, com envase e rotulagem realizadas na fábrica do instituto paulista.
Como o produto ainda não tem registro de comercialização no Brasil, sua importação fica sujeita a uma autorização excepcional da Anvisa. Na quinta-feira, o Butantã reclamou de demora na avaliação do pedido por parte da agência. O instituto afirmou que espera desde o dia 18 de setembro resposta ao pedido que fez para que a agência autorize a importação da matéria-prima da Coronavac. Segundo o Butantã, a demora impactaria “as perspectivas de produção e disponibilização de vacina contra a covid-19 para a população brasileira”.
Nesta sexta, a agência informou que autorizou “parte da solicitação” feita pelo Butantã, referente às 6 milhões de doses prontas, e disse que o processo de análise do pedido de importação da “vacina em forma de um produto intermediário, isto é, produto não envasado”, segue em tratamento e aguardando informações.
“Caso o Instituto Butantã consiga solucionar as pendências apontadas no processo da excepcionalidade, aliada a avaliação das questões técnicas relativas as boas práticas de fabricação, as quais estão em acompanhamento pela Anvisa e pelo Instituto Butantan, a Anvisa executará os trâmites para decisão dentro da maior agilidade possível”, disse a agência, em nota.
O órgão ressaltou que as 6 milhões de doses deverão ficar reservadas, “já que o produto ainda não tem registro no País e não pode ser utilizado na população”.
Whatsapp CGN 9.9969-4530 - Canal direto com nossa redação
Envie sua solicitação que uma equipe nossa irá atender você.
Participe do nosso grupo no Whatsapp
ou