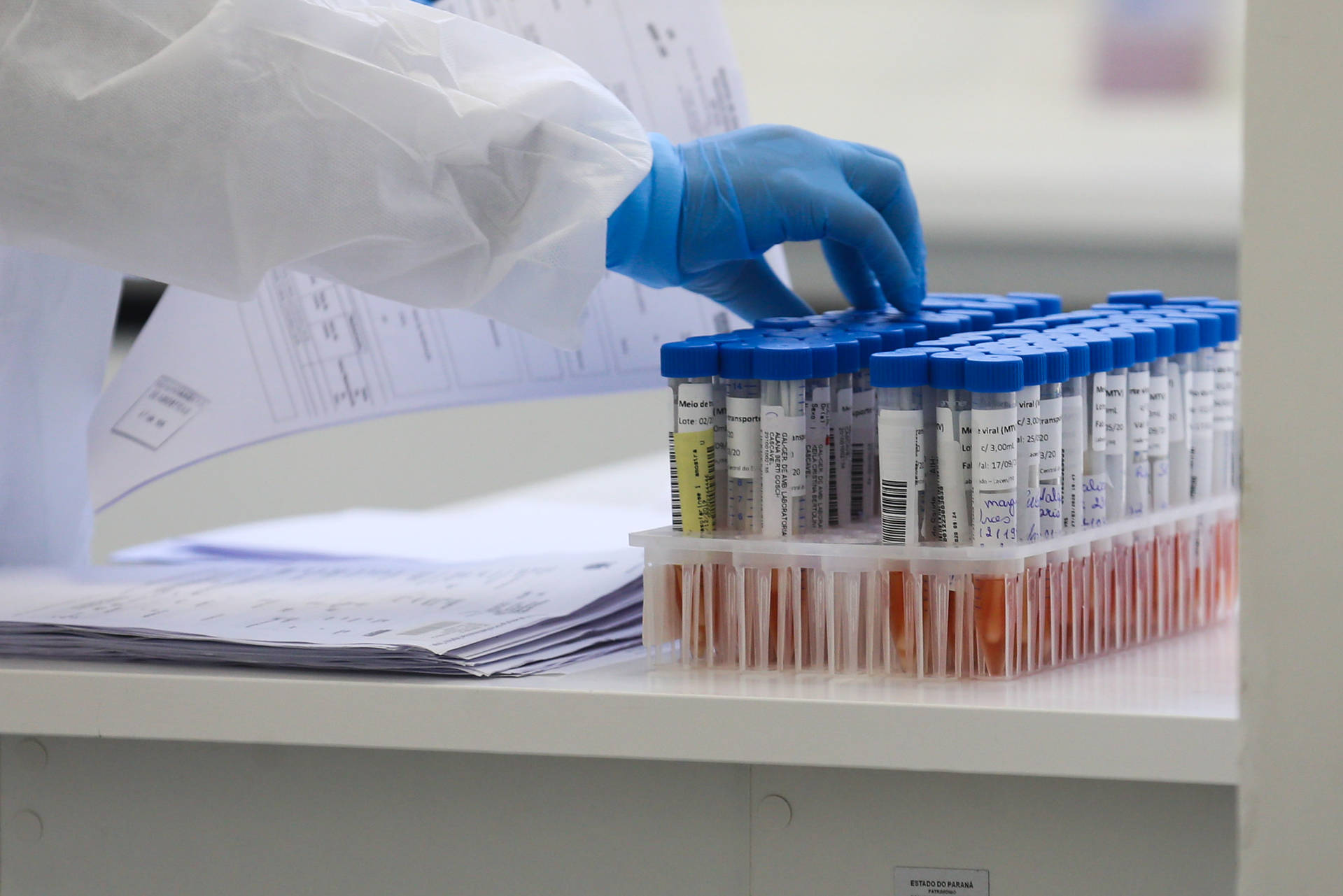
Zerada fila de pedidos de CBPF de testes para Covid-19
No total, foram analisadas 279 solicitações de certificação desde março deste ano....
Publicado em
Por CGN 1

A Anvisa zerou a fila de análise de petições de Certificação de Boas Práticas de Fabricação – CBPF para os testes para diagnóstico de Covid-19. De acordo com a Gerência Geral de Inspeção e Fiscalização Sanitária (GGFIS), a manifestação técnica final referente ao último processo que aguardava análise foi emitida no dia 06 de agosto de 2020.
De um total de quase 279 solicitações de certificação recebidas entre março e agosto deste ano, 205 foram aprovadas, 8 indeferidas e 3 encerradas.
Sessenta e três (63) petições estão em trâmite, sendo que 08 aguardam a conclusão da análise do registro conforme artigo 8º da RDC 346/2020, 02 aguardam inspeção de órgãos de vigilância sanitária local, 34 em trâmites finais de assinatura e publicação e 19 encontram-se aguardando as empresas apresentarem cumprimento de exigência técnica, quando a Anvisa solicita dados complementares ao fabricante.
Prioridade
Para possibilitar a emissão de CPBF de forma emergencial, em março deste ano a Anvisa publicou a Resolução da Diretoria Colegiada RDC 346/2020 que flexibilizou a os procedimentos de certificação de boas práticas de fabricação para fins de registro e alterações pós-registro de produtos para saúde em virtude da emergência de saúde pública internacional causada pelo novo Coronavírus.
A GGFIS passou a aceitar relatórios de inspeção de autoridades Regulatórias Estrangeiras participantes do MDSAP (Medical Device Single Audit Program); fez uso de mecanismos de inspeção remota, e de mecanismos alternativos de Certificação Temporária. As certificações temporárias foram concedidas para produtos estratégicos, a fim de atender às necessidades de saúde causadas pelo novo Coronavírus, com disponibilidade ameaçada por desabastecimento (iminente ou instalado) no mercado nacional e quando a certificação em Boas Práticas de Fabricação for o único impedimento ao registro sanitário e à comercialização do produto.
Essas medidas permitiram que um grande número de solicitações fosse avaliado em tempo recorde e tivesse prioridade de análise concedida conforme informe disponibilizado no portal da Anvisa – Esclarecimento sobre pedido de priorização de CBPF e Produtos.
A Agência informa que, por conta do atual cenário de pandemia, todos os dias há novas solicitações de avaliação de produtos, mas que está preparada para tratar com prioridade os pleitos que chegarem para análise.
Transparência
A Anvisa conta com uma plataforma de Business Intelligence (BI) da fila completa de solicitações de CBPF de produtos para diagnóstico in vitro da Covid-19. A plataforma de inteligência empresarial proporciona transparência à situação dos pedidos protocolados junto à Agência.
A plataforma permite a consulta a diversos dados, como, por exemplo, a quantidade de pedidos deferidos, indeferidos, em análise, entre outros.
Também pode ser consultada uma plataforma de inteligência que apresenta a situação de análise das petições de registro de produtos para diagnóstico in vitro da Covid-19, BI de produtos de diagnóstico in vitro para Covid-19, disponível aqui no portal.
Na plataforma de inteligência de petições de registro há 15 processos aguardando certificação, desses 07 já tiveram análise concluída e foram indeferidos, estando em etapa recursal, 03 foram concluídas e encaminhadas para publicação e 05 estão pendentes de cumprimento de exigência técnica por parte das empresas.
As informações são da Ascom/Anvisa.
Whatsapp CGN 9.9969-4530 - Canal direto com nossa redação
Envie sua solicitação que uma equipe nossa irá atender você.
Participe do nosso grupo no Whatsapp
ou